2001년 - 니시무라: Balb/c PD-1 결손 마우스에서 확인된 체액성 자가면역 기반 확장성 심근병증
발행: 2026-02-16 · 최종 업데이트: 2026-02-16
2001년 Hiroyuki Nishimura 연구는 Balb/c 배경의 PD-1 결손 마우스에서 확장성 심근병증이 발생함을 보고했습니다. 이 연구는 PD-1이 체액성 자가면역을 억제하는 핵심 면역관문임을 입증했습니다.
PD-1 결손은 항상 같은 자가면역을 일으키는가?
1998–1999년 연구에서 C57BL/6 배경의 PD-1⁻/⁻ 마우스는 시간이 지나면서 루푸스 유사 자가면역을 발병한다는 사실이 밝혀졌습니다. 그러나 면역학자들은 한 가지 중요한 점을 알고 있었습니다. 동일한 유전자 결손이라도 어떤 유전적 토양(strain background) 위에 있느냐에 따라 질병의 양상은 완전히 달라질 수 있습니다. 즉, PD-1이라는 브레이크가 사라졌을 때 터져 나오는 면역계의 약점은 개체마다 다르다는 점을 이 연구가 예견한 것입니다.
Balb/c 균주는 자가면역 감수성이 비교적 높은 계통으로 알려져 있습니다. 그렇다면 PD-1 결손이 Balb/c 배경에서는 어떤 결과를 초래할까요? 이 질문에 답한 연구가 2001년 히로유키 니시무라(Hiroyuki Nishimura) 연구팀의 보고입니다.
Balb/c 배경으로의 역교배와 생존 분석
연구팀은 PD-1 결손 유전자를 Balb/c 배경으로 10세대 이상 역교배(backcrossing)하여 유전적 배경을 안정화했습니다. 이후 생후 30주까지 생존율을 추적했습니다.
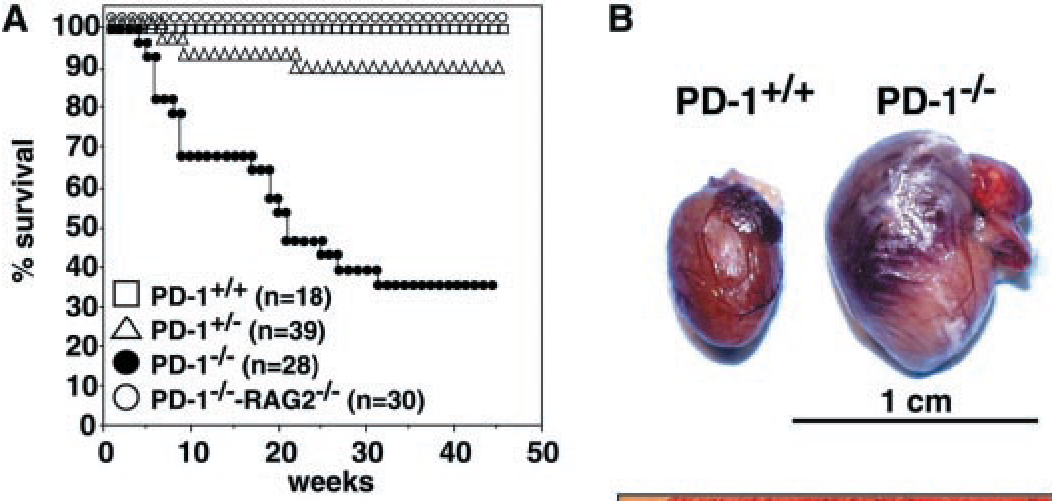
결과는 충격적이었습니다. Balb/c PD-1⁻/⁻ 마우스는 생후 5주부터 사망하기 시작했으며, 30주 이전에 약 3분의 2가 폐사했습니다. 이는 C57BL/6 PD-1⁻/⁻ 마우스가 비교적 정상 수명을 유지했던 것과 극명하게 대비되는 결과였습니다.
사망 원인은 확장성 심근병증
병리 분석 결과, 사망 개체의 심장은 전형적인 확장성 심근병증(dilated cardiomyopathy)을 보였습니다.
심근세포는 늘어나고 얇아져 있었으며, 수축 기능은 현저히 감소해 있었습니다. 이는 단순 염증이 아니라 구조적 심근 기능 상실을 의미했습니다.
33 kDa 심근 단백질에 대한 자가항체
모든 Balb/c PD-1⁻/⁻ 마우스에서 심근세포 표면의 33 kDa 단백질을 인식하는 순환성 IgG 자가항체가 발견되었습니다. 당시 연구팀이 발견한 33 kDa의 자가항원은 훗날 심근 수축 조절에 핵심적인 트로포닌 I(Troponin I)임이 밝혀지며, PD-1이 어떻게 심장 면역 관용을 유지하는지에 대한 구체적인 기전 연구로 이어지게 됩니다. 면역침착은 심근세포막과 횡문(intercalated disc) 부위에서 두드러졌습니다.
중요한 점은 조직 내 염증세포 침윤이 거의 없었다는 사실입니다.이는 세포독성 T세포가 심장을 직접 파괴하는 '심근염(Myocarditis)'이라기보다, 자가항체가 심장 기능을 마비시키는 심근병증(Cardiomyopathy)의 양상임을 보여줍니다. T세포가 직접적인 '자객'이라면, 여기서는 자가항체가 심장 엔진의 부품을 고장 내는 '방해꾼' 역할을 한 셈입니다.
CTLA-4 결손과의 대비
이 결과는 CTLA-4⁻/⁻ 마우스와 뚜렷하게 대비됩니다.
CTLA-4 결손은 T세포 폭주형 면역병리와 심근염(cardiomyositis)으로 이어지는 반면, PD-1 결손(Balb/c)은 항체 중심 체액성 자가면역과 심근병증으로 이어졌습니다.
CTLA-4가 면역계 전체의 폭발을 막는 '메인 전원 스위치'라면, PD-1은 **특정 장기에 대한 자가항체 생성을 정교하게 제어하는 '세부 조절기'**임을 이 대비가 명확히 보여줍니다.
RAG2 이중 결손에서 병리 소실
PD-1⁻/⁻ · RAG2⁻/⁻ 이중 결손 마우스에서는 심근병증이 완전히 사라졌습니다. RAG2는 T세포와 B세포의 항원수용체 재조합을 차단하므로, 이 결과는 질환이 적응면역계, 특히 항체 의존적이라는 점을 결정적으로 입증했습니다.
과학적 의의
첫째, PD-1은 B세포 및 항체 중심 자가면역을 강력하게 억제하는 핵심 분자임이 확인되었습니다.
둘째, PD-1 결손의 결과는 유전적 배경에 따라 표적 장기가 달라질 수 있다는 점이 제시되었습니다. C57BL/6에서는 루푸스 유사 신장병이 나타났고, Balb/c에서는 심장 특이적 심근병증이 발생했습니다. 이는 strain-specific autoimmunity라는 개념을 확립한 중요한 발견이었습니다.
셋째, 33 kDa 심근 자가항원을 중심으로 한 새로운 자가면역성 심근병증 모델이 제시되었습니다.
넷째, 이 연구는 이후 항-PD-1 면역항암제 치료에서 드물지만 치명적으로 나타나는 면역매개 심근염(immune-related myocarditis)의 생물학적 기반을 이해하는 데 중요한 단서를 제공했습니다.
일반인을 위한 정리
Balb/c 배경에서 PD-1을 제거하자 면역계는 자기 심장을 적으로 오해하기 시작했습니다. 염증세포가 대거 몰려오지는 않았지만, 심근세포 표면의 작은 단백질을 공격하는 자가항체가 조용히 심장을 손상시켰습니다. 심장은 점점 확장되었고 기능을 잃어갔습니다.
이 연구는 PD-1이 체액성 자가면역을 막는 중요한 방파제임을 극적으로 보여주었습니다.
참고문헌
-
Nishimura, H., Okazaki, T., Tanaka, Y., et al. “Autoimmune Dilated Cardiomyopathy in PD-1 Receptor-Deficient Mice.” Science, vol. 291, no. 5502, 2001, pp. 319–322. https://doi.org/10.1126/science.291.5502.319
-
Ishida, Y., Agata, Y., Shibahara, K., and Honjo, T. “Induced Expression of PD-1, a Novel Member of the Immunoglobulin Gene Superfamily, upon Programmed Cell Death.” EMBO Journal, vol. 11, no. 11, 1992, pp. 3887–3895. 논문 링크
-
Keir, M. E., Butte, M. J., Freeman, G. J., and Sharpe, A. H. “PD-1 and Its Ligands in Tolerance and Immunity.” Annual Review of Immunology, vol. 26, 2008, pp. 677–704. 논문 링크